科学家发现 NMN 用于恢复 NAD+ 水平的 SLC12a8 通路

是的,NMN 可以完整地穿过细胞膜
这项刚刚发表的研究发现了一种名为 Slc12a8 的酶,它可以将少量的烟酰胺单核苷酸 (NMN) 直接输送到某些细胞中
然而,这种酶只普遍存在于年龄较大、病情较重的动物和人类的小肠中。
Slc12a8 酶之所以刚刚被发现,是因为它起的作用非常小,并且不会运输足够多的 NMN,因此之前没有注意到。
少量NMN胶囊有时可以绕过肝脏
人们早就注意到,少量的 NMN 可以在几分钟内到达血液。2019 年 1 月发表的一项研究揭示了这种情况的答案, 该研究表明新发现的Slc12a8 蛋白可以将 NMN 转运到小肠中的 NAD+,避免被 NAM 消化。
这似乎不是一个重要的数额
该研究没有公布显示 Slc12a8 酶可以运输多少 NMN 的结果,但所有先前的研究(例如Liu 的研究) 根本找不到通过该途径产生的任何 NAD+ 的证据。
根据作者的说法:
重要的是要注意,NMN 转运蛋白的发现绝不会降低通过去磷酸化摄取的重要性
还必须注意的是,Slc12a8 转运蛋白在小肠中最为突出,但没有通往身体其他部位的通路。
希望 Slc12a8 能在未来的产品中发挥作用
未来的产品可能会很快投放市场,以这一途径为目标,以帮助解决 NMN 胶囊的生物利用度问题。根据研究:
“今井博士的实验室已经确定了可以刺激 Slc12a8 NMN 转运蛋白产生的小分子,申请了专利,并将这项技术授权给了日本的一家公司”
不过现在,您可以通过舌下服用来避免 NAD+ 或 NMN 被消化——更多关于舌下给药的信息——
有关该研究的更多详细信息
小肠中的 Slc12a8 对于将 NMN 从肠道转运到循环中很重要,它会影响小肠中的 NAD+ 水平和体内的全身 NMN 供应。
值得注意的是,与年轻人相比,Slc12a8 NMN 转运蛋白的功能在老年人中变得至关重要。为了响应 NAD+ 水平的显着降低,老化的回肠上调 Slc12a8 表达并试图维持其 NAD+ 水平
当提供足够的 NMN 时,该反馈系统可以充分发挥作用,以维持与年轻人相当的 NAD+ 水平
这项发表于 2019 年 1 月 7 日的研究解决了多年来一直是该领域科学家激烈猜测焦点的谜团——NMN 如何进入细胞以变成 NAD+,并且它不需要转化为 NR(烟酰胺核苷)这样做。
由医学博士今井新一郎领导的位于圣路易斯的华盛顿大学医学院的科学家们 发现,Slc12a8 蛋白可以快速将 NMN 直接转运到细胞中。
这项研究的一些重要发现:
- Slc12a8 转运蛋白为细胞内的 NAD+ 提供快速、直接的途径
- 途径特定于 NMN——不适用于 NR、NAMN 或其他代谢物
- 在老年动物中上调以补偿 NAD+ 减少
- 刺激 Slc12a8 转运蛋白可能会增加细胞中的 NAD+
- 在小肠、肝脏、胰腺和脂肪细胞中最为普遍
- 对胶囊形式的 NMN 补充剂的影响未量化
NMN 在细胞内快速、直接的运输
在这项研究之前,一些研究人员认为 NMN 不能完整地穿过细胞膜。他们声称NMN 穿过细胞膜的唯一方法是首先转化为 NR,穿过细胞膜,然后再转化回 NMN,再转化为 NAD+。
Imai 博士和他的团队长期以来一直怀疑 NMN 有一条直接进入细胞的途径,因为 NMN 从肠道进入血液,然后在几分钟内进入全身细胞,这比在 NR 研究中观察到的要快得多,所以Imai 博士确信必须有一条从外部 NMN 穿过细胞膜的直接途径。
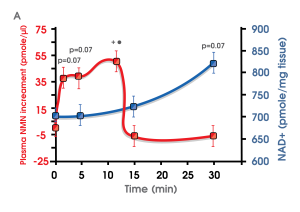
在 Imai 博士及其团队于 2016 年发表的这项早期研究中,给小鼠注射了单剂量的 NMN 水溶液。
血液中的 NMN 水平显示它在 2'“3 分钟内迅速从肠道吸收 进入血液循环 ,然后在 15 分钟内从血液循环中清除并在比目鱼肌细胞内转化为 NAD
Slc12a8 可能是 NMN 摄取如此迅速地转化为 NAD+ 的原因。
目前的研究发现,具有“敲低”Slc12a8 基因 (Slc12a8-KD) 的小鼠没有同样快速的利用。
“NMN 的快速摄取在Slc12a8敲低 ( Slc12a8 -KD) 肝细胞中被完全消除,而在Nrk1敲低 ( Nrk1 -KD) 肝细胞中未观察到 NMN 摄取显着减少(图1f),这表明Slc12a8是必需的因为 NMN 在原代肝细胞中的快速摄取,并且观察到的细胞内 NMN 的增加不是由于 NR 或烟酰胺转化为 NMN。”
此外,缺失 Slc12a8 基因的小鼠在 NAD+ 合成中处于不利地位:
全身 Slc12a8-KO 小鼠在直接、分钟级 NMN 运输和 NAD+ 生物合成中显示出显着缺陷
途径特定于 NMN – 不适用于 NR
研究人员使用 NMN、NR 和其他 NAD+ 代谢物的双标记分子来追踪细胞的摄取。
用 NMN 处理过表达 Slc12a8 基因的细胞会导致细胞内摄取大约 4 倍以上的 NMN。
用 NR 处理相同的细胞会导致细胞内 NMN 的 NO 增加。
事实上,即使与 NMN 几乎相同的 NAMN 也没有被转运到细胞中,这证实了这种转运蛋白对于携带 NMN 穿过细胞膜具有特异性。
“在这里,我们表明 Slc12a8 基因编码了一种特定的 NMN 转运蛋白。“
“我们进一步表明 Slc12a8 专门转运 NMN,但不转运烟酰胺核苷”
刺激 Slc12a8 转运蛋白增加 NAD+
研究人员能够刺激 Slc12a8 基因以“提高”Slc12a8 蛋白的数量。该图表显示了在“过度表达”该基因的细胞中发现的增加的 NMN。
b ,在对照和 Slc12a8-OE NIH3T3 细胞中摄取 3 H-NMN(25 μM,37 °C)( n = 12 个生物学独立样本;通过方差分析和 Sidak 检验进行分析,* P = 0.0136,*** P = 0.0001 ).
考虑到这一点,Imai 博士的实验室已经确定了可以刺激 Slc12a8 NMN 转运蛋白产生的小分子,申请了专利,并将这项技术授权给了一家名为 Teijin Limited 的日本公司。
在老年动物中上调以补偿 NAD+ 减少
给小鼠口服 500 mg/kg NMN 后,老年小鼠小肠细胞内 NAD+ 水平高于年轻小鼠,表明 Slc12a8 的上调在抵消与年龄相关的小肠 NAD+ 下降中起重要作用肠。
“响应 NAD+ 下降,Slc12a8 基因的表达上调,使细胞能够满足对 NAD+ 生物合成的迫切需求”
在小肠、肝脏、胰腺和脂肪细胞中最为普遍

b,在对照小鼠和 Slc12a8 -KD 小鼠(n = 6 只小鼠;3-4 个月大的 B6 雄性;通过 Sidak 检验进行方差分析分析,* * P = 0.0080)。
他们的大部分测试都是在小肠进行的,因为那里是 Slca18 最丰富的地方,但在肝脏、胰腺和脂肪细胞中也有发现:
“Slc12a8 在小肠和胰腺中高表达,在肝脏和白色脂肪组织中中度表达”
他们还对肝细胞进行了一些研究,表明 Slc12a8 敲除后 NMN 摄取减少了 90%:
当用 100 μM O18-D-NMN 处理时,Slc12a8- KO 肝细胞在 5 分钟时与对照野生型肝细胞相比,O18-D-NMN 摄取减少约 90%
与早期研究的矛盾?
2018 年 3 月发表的这项研究(Liu,Rabinowitz)表明,几乎所有口服的 NMN 和 NR 都会在胃肠道和肝脏中降解为 NAM,没有一个会完整地输送到肝脏外。
这似乎与本研究中的发现相反,该研究表明口服管饲有效地将 NMN 输送到细胞内并迅速转化为 NAD+
有几点可以解释这种表面上的差异:
- Liu 的研究使用的是相当年轻的老鼠。Slc12a8 转运蛋白在年轻动物中不使用/不需要
- Liu 的研究没有公布服用 NMN 后小肠中 NAD+ 水平的数据
- Imai 博士指出,这项最新研究立即测量了血液中的 NAD+ 代谢物,正如他们所说,冷冻和解冻血液(这是 Liu 研究中所做的)会破坏一些 NAD+ 代谢物
问题依然存在
这种专用的 NMN 转运蛋白的发现很有趣,但是
这项研究并没有试图量化通过 Slc12a8 转运蛋白使其成为 NAD+ 完整的 NMN。
作者并不以任何方式暗示所有 NMN 补充剂都可以利用这一途径。
Sinclair 博士在对 Imai 研究的评论中说:
重要的是要注意,NMN 转运蛋白的发现绝不会降低通过去磷酸化摄取的重要性
我们不知道:
- 多少百分比的 NMN 补充剂在到达小肠之前可能会在胃中降解。
- 进入小肠的 NMN 中有多少百分比能够利用这种转运蛋白?
- 从小肠成功转化为 NAD+ 的 NMN 中有多少供应身体的其他组织?
- 在 Slc12a8 转运蛋白不堪重负之前可能有用的 NMN 剂量范围是多少?
- 可以做些什么来刺激更多的 Slc12a8 ?
为什么我们需要为 NMN 使用舌下递送

我们对 NAD+ 生物学的了解不断增长,毫无疑问,随着 NAD+ 故事的不断发展,未来还会有更多的惊喜。
我们现在有证据表明存在一种专用的 NMN 转运蛋白,它在老年动物中上调以补偿低 NAD+ 水平,这可能是 NMN 被发现在细胞内代谢为 NAD+ 的速度比 NR 快得多的原因。
但我们不知道任何 NMN 补充剂中有多少百分比能够利用这种途径产生 NAD+。
我们也不知道身体将 NAD+ 从小肠转移到全身其他组织的效率如何。
NMN 不需要 Slc12a8 进入细胞。它是 NMN 特有的替代途径,在小肠、肝脏和胰腺中最为普遍。
在某些没有 Slc12a8 的细胞中,NMN 需要失去一个磷酸盐(转化为 NR)才能进入。但是,这并不妨碍它进入。
NMN 使用一种在细胞膜上很容易找到的蛋白质来丢弃磷酸盐。
它并不是 Chromadex 喜欢描绘的真正不可逾越的进入障碍,而更像是一个检查站。可能就像你在朋友家一样,进入之前需要脱鞋。
在试管中,NR 进入细胞的速度更快。但在体内,情况并非如此。在水中或强饲法中,它们以相同的速度在肝脏中增加几乎相同数量的 NAD+。
舌下含服 NMN 可能会在几分钟内将 30% 左右放入血液中,在那里它可以进入全身细胞。如果您吞下一粒 NR 胶囊,需要一个小时或更长时间才能通过肝脏,然后一些非常小的百分比才能到达血流。
现在我们知道,使用 Slc12a8,一部分 NMN 可以在小肠中转化为 NAD+,比肝脏中的 NR 快得多。但我们不知道那是多少,而且可能有很大的差异。
结论

在这一新发现之前,人们普遍认为 NMN 不能直接进入细胞,必须转化回 NR 才能进入。
我们现在知道这不是真的,而且肯定有一个专门针对 NMN 的专用转运蛋白。
没有 Slc12a8 转运蛋白,NMN 胶囊会遭遇与 NR 相同的命运,并且在胃和肝脏中几乎完全被 NAM 消化(Liu,Rabinowitz)
如果 Slc12a8 蛋白受到刺激(如在老年动物中),则其中一些 NMN 可以完整地直接运输到细胞中并增加 NAD+。
然而,没有理由相信 Slc12a8 可以处理所有通过小肠和肝脏的 NMN——舌下含服胶囊可能更有效。


